|
|
 |
| Авторизация |
|
|
 |
| Поиск по указателям |
|
 |
|
 |
|
|
 |
 |
|
 |
|
| Мецлер Д. — Биохимия. Химические реакции в живой клетке (том 3) |
|
|
 |
| Предметный указатель |
Сукцинатдегидрогеназа, флавин и железо-сериые группы II: 266
Сукцинаттиокиназа (сукцинил-CoA — синтетаза) II: 135—-136
Сукцинил-CoA II: 138; 318с; III: 101
Сукцинил-CoA : ацетоацетат — CoA-трансфераза II: 138
Сукцинил-CoA в биосинтезе II: 457 458
Сукцинил-CoA в катаболизме пропионата II: 333
Сукцинил-CoA в пропионовокислом брожении II: 352
Сукцинил-CoA в цикле трикарбоновых кислот II: 318с 319 323 325
Сукцинил-CoA как предшественник гема III: 123
Сукцинил-CoA — синтетаза (сукцииат-тиокиназа) II: 135—136
Сукцинил-CoA, конденсация с глицином II: 218 488
Сукцинил-CoA, образование GTP II: 334
Сукцинил-CoA, превращение в 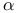 -кетоглутарат II: 472 475 -кетоглутарат II: 472 475
Сукцинилирование III: 107—108
Сукцинилированная форма изоцитрат-лиазы II: 170
Сукциниловые группы в липополисахариде I: 178
Сукцинилфосфат II: 136
Сульфаминовая кислота, производные II: 139
Сульфаниламид II: 33с
Сульфаниламид, ацетилирование II: 190с
Сульфат, активный II: 139
Сульфатазы II: 88 140 544
Сульфатазы в липидах I: 147
Сульфатазы как неорганический окислитель II: 425
Сульфатазы, восстановление II: 434; III: 132
Сульфатазы, восстановление с помощью 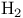 II: 432 II: 432
Сульфатазы, выделение III: 135
Сульфатазы, недостаточность II: 541
Сульфатазы, поглощение I: 359
Сульфатазы, потенциал восстановления II: 432
Сульфатазы, этерификация III: 135
Сульфатиды I: 341
Сульфатные группы, перенос II: 139—140 536
Сульфгидрилсодержащие ферменты II: 151
Сульфгидрильные (—SH) группы II: 250
Сульфгидрильные (—SH) группы в кофермеите A II: 191 193
Сульфгидрильные (—SH) группы, связь с протогемом II: 365
Сульфид, включение III: 132
Сульфид, окисление у Thiobacillus II: 428—429
Сульфит III: 132
Сульфит, окисление в сульфат II: 428—429
Сульфит, присоединение к флавинам II: 261
Сульфит-цитохром-с—редуктаза II: 429
Сульфитоксидаза II: 428 430
Сульфитоксидаза дефектная III: 135
Сульфитоксидаза и цитохром III: 135
Сульфитоксидаза, содержащая вольфрам III: 86
Сульфитоксидаза, содержащая молибден III: 85 135
Сульфитредуктаза II: 433; III: 132
Сульфитредуктаза сирогем II: 432; III: 132
Сульфокиназы II: 139
Сульфолактальдегид III:. 135с
Сульфолактальдегид при образовании сульфолипида III: 134
Сульфолипид I: 150с 151 341; 134
Сульфолипид в хлоропластах I: 151; III: 41 45
Сульфонамиды II: 33 (см. также «Сульфаниламид»)
Сульфонамиды, блокирование синтеза пуринов III: 170
Сульфонатзамещениый полистирол I: 165
Сульфонаты в липидах I: 147
Сульфоний-'ион, нуклеофильное замещение II: 93
Сульфотрансферазы II: 88 139
Сульфоэфирные группы, перенос II: 139
Сульфурилаза II: 464
Суммарная степень окисленности II: 473
Супероксид-анион II: 268 274 366 436 438 440
Супероксид-анион в реакциях гидроксилирования II: 435
Супероксид-анион, ксантиноксидаза II: 268
Супероксиддисмутаза II: 287 448—449
Супероксиддисмутаза, ингибирование II: 435—436
Супероксиддисмутаза, содержащая марганец III: 52
Супероксиддисмутаза, содержащая цинк II: 142
Суперпреципитация I: 324
Суперскрученность см. «Суперспираль»
Суперспирализация ДНК, влияние гистонов III: 303
Суперспираль I: 92
Суперспираль ДНК I: 139; III: 257
Суперспираль жгутиков I: 276 282
Суперспираль пептидных цепей I: 132
Супрессия nonsense-мутаций III: 253
Супрессия, внутригеииая III: 255
Супрессия, эффективность III: 256
Супрессорные amber III: 188 243 254
Супрессорные ochre III: 188
Супрессорные sup F (su-3) III: 254
Супрессорные sup F (su-3), тирозиновая тРНК III: 220
Супрессорные гены III: 243 254 255
Сурфактии I: 86c
Сурьма I: 155
Суточные циклы, действие света III: 68—69
Сферопласт I: 22
Сфинганин см. «Сфингозин»
Сфинганин (дигидросфингозии) II: 560с
Сфинганин (сфингенин) I: 148с; II: 560
Сфинганин (сфингенин), биосинтез II: 219 488
Сфинганин (сфингенин), катаболизм II: 560
Сфинганин (сфингенин), серии III: 118
Сфинголипидозы II: 542 543 544
Сфинголипиды I: 152 173;
Сфинголипиды, биосинтез II: 543 (схема) 560
Сфинголипиды, катаболизм II: 543 (схема)
Сфинголипиды, свойства II: 560
Сфингомиелииаза II: 544
Сфингомиелины I: 149 152с 341
Сфингомиелины в мембранах I: 351 352
Сфингомиелины, биосинтез II: 542 543
Сыворотка крови, концентрация кальция I: 373
Сыворотка крови, электрофорез I: 164
Сывороточный альбумин I: 103
Т-трубочки I: 320 325;
Таламус III: 319 328
Таллий I: 155
Талоза I: 108
Таннины конденсированные III: 151—152
Таннины, гидролизуемые III: 151
Тапетум, рибофлавин, II: 256
Тапетум, цинк II: 143
Тараканы, углеводороды II: 551
Таурин III: 131с
Таурин как ингибитор нейронов III: 340
Таурин как нейромедиатор III: 335
Таурин, функция в фоторецепторных клетках сетчатки III: 134
Таурохолевая кислота II: 583с 584
Таутомеразы II: 154
Таутомеризация II: 481 (см. также «Таутомерия»)
Таутомеризация в синтезе пуринов III: 168
Таутомериое отношение I: 79 255
Таутомериое отношение, спектрометрическое определение I: 255
Таутомериые переходы в парах оснований III: 214
Таутомериый катализ II: 55 110
Таутомерия I: 77—79 255—256;
Таутомерия 1-метилурацила I: 256
Таутомерия амидов I: 77—78
Таутомерия глутатиона I: 256; II: 179
Таутомерия и спаривание оснований I: 138
Таутомерия имидазольной группы I: 79
Таутомерия кето-енольная I: 77
Таутомерия пиридоксииа I: 78
Таутомерия порфиринов II: 365
Таутомерия при образовании меланина III: 148
Таутомерия при связывании лигандов с белками I: 256
Таутомерия урацила I: 78
Таутомерия цистеииа I: 256
Таутомерия, константы равновесия I: 79
Таутомеры см. «Таутомерия»
Таутомеры биполярные ионные I: 78
Таутомеры минорные III: 214
Таутомеры минорные как причина мутаций III: 247
Таутомеры минорные тиаминднфосфата II: 204
Тейхоевые кислоты I: 394—395
Тейхоевые кислоты в клеточных стенках I: 394
| Тейхоевые кислоты, синтез II: 494
Тектин I: 352
Теллурий, метилирование II: 298
Теллурий, токсичность I: 155
Тело нейрона III: 325
Телофаза III: 264 266
Температура перехода мембран I: 343
Температура, влияние на гидрофобное взаимодействие I: 249
Теноилтрифторацетон II: 397 398
Тенуазоновая кислота II: 594с
Теория графов II: 23
Теория ключа и замка II: 42
Теория Кноопа, 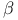 -окисления II: 311 -окисления II: 311
Теория переходного состояния II: 48—49
Теория рецепторов II: 32
Теплота I: 201 202—203
Теплота сгорания I: 202 203
Теплота, генерация II: 403
Тератогенная активность диоксина III: 129
Тербий(III) как флуоресцентный зонд III: 32
Терминальные пластинки I: 58
Терминаторы в гемоглобииовых генах III: 364
Терминацня белкового синтеза III: 231 234 236
Терминирующие кодоны III: 192 193 243
Терминирующие кодоны в MS2 РНК III: 242
Терминирующие кодоны, дублирование III: 236
Термиты, простейшие I: 44
Термогенная ткань в растениях II: 404
Термогенная ткань, бурая жировая II: 403
Термодинамика I: 200—241
Термодинамика жизнедеятельности I: 232—234
Термодинамика необратимых процессов I: 233
Термодинамика неравновесных процессов I: 233
Термодинамика транспорта электронов II: 406—409
Термодинамика, второй закон I: 205—208
Термодинамика, первый закон I: 201—205
Термодинамическая температурная шкала I: 205
Термодинамические барьеры в биосинтезе II: 491
Термолизин I: 101
Термолизин,  I: 375 I: 375
Термолизин, Тербий в кальцийсвязывающем центре III: 32
Термолизин, флуоресцентный зонд III: 32
Терморегулятор I: 64
Термохимия I: 202
Терпены I: 146; II: 56Т—574
Терпены, биосинтез II: 563 567—568
Терпены, структура II: 56
Терпингидрат II: 568
Тест на восстановление ацетилена III: 82
Тестостерон II: 585с; 589; III: 321
Тетрагидробиоптерин II: 438с
Тетрагидроканнабинол III: 347
Тетрагидрофолиевая кислота ( ) II: 218 275—283 278с 330 434 478 ) II: 218 275—283 278с 330 434 478
Тетрагидрофолиевая кислота ( ) при декарбокоилированнн глицина III: 121 ) при декарбокоилированнн глицина III: 121
Тетрагидрофолиевая кислота ( ), биосинтез III: 174 (схема) ), биосинтез III: 174 (схема)
Тетрагидрофолиевая кислота ( ), конфигурация II: 277 ), конфигурация II: 277
Тетрагидрофолиевая кислота ( ), одноуглеродные производные II: 280 (схема) ), одноуглеродные производные II: 280 (схема)
Тетрагидрофолиевая кислота ( ), перенос формила III: 160 ), перенос формила III: 160
Тетрагидрофолиевая кислота ( ), сопряженные соединения II: 277 ), сопряженные соединения II: 277
Тетрагидрофолилтриглутаминовая кислота ( -триглутаминовая кислота) II: 277 (см. также «Тетрагидрофолиевая кислота») -триглутаминовая кислота) II: 277 (см. также «Тетрагидрофолиевая кислота»)
Тетрагидрофолилтриглутаминовая кислота ( -триглутаминовая кислота) у Clostridium II: 278 -триглутаминовая кислота) у Clostridium II: 278
Тетрагидрофолилтриглутаминовая кислота ( -триглутаминовая кислота), биосинтез III: 1174 (схема) -триглутаминовая кислота), биосинтез III: 1174 (схема)
Тетрагональная бипирамида как переходное состояние при псевдовращении II: 123
Тетрада III: 266
Тетрада, анализ III: 286
Тетрадекановая кислота (миристиновая кислота) I: 149
Тетрадотоксин I: 371 593; III:
Тетрадотоксин, блокирование натриевых каналов III: 334
Тетразолиевая соль II: 401
Тетракозановая кислота (лигиоцерниовая кислота) I: 149
Тетрамер I: 270
Тетрамерный фермент I: 281
Тетраметил-n-фенилендиамин II: 401с
Тетраметил-n-фенилендиамин в транспорте электронов II: 400
Тетраметилглюкоза, мутаротация II: 54
Тетраметилсилан I: 185
Тетранитрометан, реакция с альдолазой II: 165
Тетранитрометан, реакция с тирозильными группами II: 165
Тетрануклеотид, гипотеза структуры нуклеиновой кислоты III: 183
Тетрапирроллы водорослей III: 44 131
Тетрапиррольные пигменты, с открытой цепью III: 130
Тетраплоидные организмы III: 267
Тетрациклины I: 367; II: 562с; III: 240
Тетрациклины, биосинтез II: 563
Тетрациклины, влияние на «stringent»-ответ III: 246
Тетраэдр I: 285
Тетраэдрическое расположение субъединиц I: 280
Тетраэтилпирофосфат II: 105с
Тефлон (полифторэтилеи) I: 87
Тиазолидиновый цикл II: 224
Тиамиитетрафосфат II: 207
Тиамин II: 207—209
Тиамин в метаболизме глиоксилата III: 120
Тиамин как гормон роста корней III: 324
Тиамин, аддукты II: 202
Тиамин, аналоги II: 209
Тиамин, анион желтого цвета I: 281; II: 208
Тиамин, вытеснение из нервных клеток II: 209
Тиамин, деградация с помощью щелочи II: 208
Тиамин, дезаминирование II: 209
Тиамин, кислотно-основные свойства I: 261; II: 207—208
Тиамин, кооперативное связывание протонов I: 262
Тиамин, образование пиримидинового кольца III: 170
Тиамин, пиримидиновая часть II: 225
Тиамин, расщепление бисульфитом II: 93
Тиамин, расщепление сульфитом II: 209—209
Тиамин, содержание в организме человека II: 451
Тиамин, тиол II: 208
Тиамин, трициклическая форма I: 261; II: 208
Тиамин, ферментативные реакции II: 205
Тиаминазы II: 209
Тиаминдифосфат II: 201—209 202с 240 270 275 341 473 490; 113
Тиаминдифосфат в 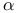 -расщеплении II: 202 307 -расщеплении II: 202 307
Тиаминдифосфат в образовании О-сукцинилбензоата III: 143
Тиаминдифосфат в цикле дикарбоновых кислот II: 328
Тиаминдифосфат, механизм действия II: 203—209
Тиаминдифосфат, рентгеноструктурные исследования II: 204
Тиаминдифосфат, система «переноса заряда» II: 204
Тиаминмонофосфат II: 442
Тиаминовые коферменты в нейронах II: 209
Тиаминовые коферменты в транспорте натрия II: 209
Тиаминпирофосфат см. «Тиаминдифосфат»
Тиаминтрифосфат II: 207
Тиаминтрифосфатазы II: 209
Тивелоза I: 391с
Тилакоиды в хлоропластах III: 44—46 54
Тимидилат-синтетаза III: 164 165—166
Тимидилат-синтетаза в хемотерапии рака III: 165
Тимидин I: 126
Тимидин радиоактивный III: 166 196
Тимидин, ингибирование синтеза ДНК III: 163
Тимидин, фосфорилирование III: 1166
Тимин I: 123 126 168
Тимин радиоактивный III: 166
Тимин расщепление III: 167
Тимин фолатные коферменты II: 279
Тимин фотодимеризация III: 36
Тимин фотохимические превращения I: 138
Тимин, замена на бромурацил III: 272
Тимндиловая кислота (dTMP), образование из dUMP III: 164
Тимозии III: 365
Тимол II: 568с
Тимус, гистоны III: 302
Тимус, развитие T-клеток III: 302
Тимьян, содержание тимола II: 568
Тиогалактозид-трансацетилаза, ген III: 187
Тиоглутатион III: 135
Тиолазы II: 162 308
Тиолиз II: 309
Тиоловые группы I: 176
|
|
 |
| Реклама |
 |
|
|
 |
|
О проекте
|
|
О проекте



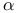 -кетоглутарат
-кетоглутарат 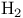
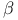 -окисления
-окисления 
 )
)