Авторизация
Поиск по указателям
Харнед Г., Оуэн Б. — Физическая химия растворов электролитов
Обсудите книгу на научном форуме Нашли опечатку?
Название: Физическая химия растворов электролитовАвторы: Харнед Г., Оуэн Б. Аннотация: Книга Харнеда и Оуэна состоит из пятнадцати глав и двух приложений и может быть, по существу, разделена на три части. Первая часть (гл. I—V) посвящена всестороннему изложению теории междуионного взаимодействия, причем в гл. V даны краткое обобщение всего этого раздела и теоретические уравнения, выраженные в форме, наиболее удобной для их экспериментальной проверки. Вторая часть (гл. VI—X) содержит изложение принципиальных основ экспериментальных методов исследования свойств растворов электролитов (электропроводности, вязкости, диффузии, парциальных молярных величин, температур замерзания и кипения, упругости пара). Дан подробный обзор экспериментальных результатов и методов их обработки, а также сопоставление их с теоретическими. Наконец, третья часть (гл. XI—XV) по¬священа описанию термодинамических свойств растворов конкретных веществ (соляной кислоты, 1,1-валентных и поливалентных электролитов, а также смесей сильных электролитов). Здесь же рассматриваются константы диссоциации отдельных слабых электролитов и их смесей. В приложении А даны таблицы, иллюстрирующие экспериментальный материал, приведенный в тексте книги. В приложении Б, введенном авторами во второе издание, даны исправленные значения некоторых величин, а также сделаны краткие добавления к первому изданию.
Язык: Статус предметного указателя: Готов указатель с номерами страниц ed2k: ed2k stats Год издания: 1952Количество страниц: 629Добавлена в каталог: 20.09.2006Операции: Положить на полку |
Скопировать ссылку для форума | Скопировать ID
Предметный указатель
469 487 205 476 478 541 545 dl- 476 dl- 476 dl- 544 dl- 546 dl- 544 dl- 546 dl- 476 dl- 476 dl- 544 dl- 546 dl- 544 dl- 546 dl- 476 dl- 476 dl- 544 dl- 546 dl- 544 dl- 546 dl-Аланин, изменение термодинамических функций при кислотной диссоциации 476 dl-Аланин, изменение термодинамических функций при основной диссоциации 476 dl-Аланин, константа кислотной диссоциации 541 544 dl-Аланин, константа кислотной диссоциации максимальная 546 dl-Аланин, константа кислотной диссоциации, определение 471 dl-Аланин, константа основной диссоциации 541 544 dl-Аланин, константа основной диссоциации максимальная 546 dl-Валин, изменение термодинамических функций при кислотной диссоциации 476 dl-Валин, изменение термодинамических функций при основной диссоциации 476 dl-Валин, константа кислотной диссоциации 544 dl-Валин, константа кислотной диссоциации максимальная 546 dl-Валин, константа основной диссоциации 544 dl-Валин, константа основной диссоциации максимальная 546 dl-Изолейцин, изменение термодинамических функций при кислотной диссоциации 476 dl-Изолейцин, изменение термодинамических функций при основной диссоциации 476 dl-Изолейцин, константа кислотной диссоциации 544 dl-Изолейцин, константа кислотной диссоциации максимальная 546 dl-Изолейцин, константа основной диссоциации 544 dl-Изолейцин, константа основной диссоциации максимальная 546 dl-Лейцин, изменение термодинамических функций при кислотной диссоциации 476 dl-Лейцин, изменение термодинамических функций при основной диссоциации 476 dl-Лейцин, константа кислотной диссоциации 544 dl-Лейцин, константа кислотной диссоциации максимальная 546 dl-Лейцин, константа основной диссоциации 544 dl-Лейцин, константа основной диссоциации максимальная 546 dl-Норлейцин, изменение термодинамических функций при кислотной диссоциации 476 dl-Норлейцин, изменение термодинамических функций при основной диссоциации 476 dl-Норлейцин, константа кислотной диссоциации 544 dl-Норлейцин, константа кислотной диссоциации максимальная 546 dl-Норлейцин, константа основной диссоциации 544 dl-Норлейцин, константа основной диссоциации максимальная 546 o-Нитробензойная кислота, константа диссоциации 577 o-Нитробензойная кислота, коэффициенты высаливания 529 o-Толуиловая кислота, коэффициенты высаливания 529 o-Хлорбензойная кислота, константа диссоциации, определение методом электропроводности 205 pH некоторых стандартных растворов, таблица 306 pH, определение 302—306 pH, определение постоянной уравнения, таблица 305 pH, уравнение 303 (см. «также Концентрация водородных ионов») Адамс, Е. 496 Адамс, Л. 249 258 267 269 283 Аделл 306 310 486 496 497 Адсорбционный потенциал, определение 70—71 Азот, закись см. «Закись азота» Азотная кислота, степень диссоциации, таблица 576 Айзер 379 385 Айрес 235 239 240 266 268 Акерлёф 73 119 137 228 265 310 311 315 322 324 330 337 338 351 352 375 384 385 386 390 416 430 432 436 438 444 446 447 522 523 551—553 Акри 302 310 552 590 Аксельрод, Н.В. 444 Активность воды в растворе серной кислоты, определение 408—410 Активность выражение через моляльность 27 Активность выражение через молярность 27 Активность гидратированных ионов 573 Активность ионов средняя, определение 24 Активность компонента системы 25 Активность негидратированных ионов 573 Активность раствора, уравнение 275 Активность растворителя, вычисление из данных для температур замерзания, уравнение 270—272 Активность растворителя, вычисление из данных для температур кипения, уравнение 273—274 Активность растворителя, вычисление по измерениям давления пара, уравнение 274—276 Активность растворителя, вычисление по изопиестическим данным, уравнение 274—276 Активность электролита 23—24 Активность, зависимость от состава 26 Активность, зависимость от температуры и давления 25 Активность, коэффициент см. «Коэффициент активности» Активность, свойства 27 Активность, уравнение 24 Алюминий сернокислый, высаливание нейтральных молекул 376 Алюминий сернокислый, коэффициент активности средний 402 Алюминий хлористый, высаливание нейтральных молекул 376 Алюминий хлористый, коэффициент активности 534 Амальгамные элементы см. «Элементы амальгамные» Аммоний азотнокислый, высаливание нейтральных молекул 376 Аммоний азотнокислый, кажущийся молярный объем 242 Аммоний азотнокислый, коэффициент активности, средний при температурах замерзания водных растворов 504 Аммоний азотнокислый, парциальный молярный объем, влияние давления 250 Аммоний бромистый, коэффициент активности, средний при температурах замерзания водных растворов 504 Аммоний йодистый, коэффициент активности, средний при температурах замерзания водных растворов 504 Аммоний сернокислый, коэффициент активности, средний при температурах замерзания водных растворов 504 Аммоний хлористый, кажущееся относительное молярное теплосодержание 500 Аммоний хлористый, кажущийся молярный объем 242 Аммоний хлористый, коэффициент активности, средний при температурах замерзания водных растворов 504 Аммоний хлористый, относительное парциальное молярное теплосодержание 502 Аммоний хлористый, числа переноса 499 Аммоний хлористый, эквивалентная электропроводность 498 Амфолиты, константы диссоциации 548 Амфолиты, константы диссоциации, определение 469—472 Амфолиты, коэффициенты активности 470—471 Анваер, Б. 226 Андауэр 268 549 Андерсон, Н. 508 550 Андерсон, Р. 576 588 Ансон 180 Аргон, коэффициент высаливания 528 Аргон, различные солевые эффекты 377 Армстон 429 447 Аррениус 179 180 201 215 450 495 Асбах 267 Асмус, Е. 181 Ассоциация ионов, теория Бьеррума 54—57 Астин 137 177 Астон 181 549 Атмосфера иона, мера относительной несимметричности 85 Атмосфера иона, уравнение, теория Дебая 38—42 Ацетат ион, гидролиз в растворах хлористых солей, таблица 448—489 Ацетилен, коэффициенты высаливания 528 Ацетон, высаливание и всаливание различными солями 379 Бакстер, Г. 242 266 Бакстер, У. 419 447 Балансное детекторное устройство 139 Балке 283 Барак 178 Барий азотнокислый, кажущееся относительное молярное теплосодержание 501 Барий азотнокислый, константа диссоциации иона 149 Барий азотнокислый, коэффициент активности средний 570 Барий азотнокислый, относительное парциальное молярное теплосодержание 503 Барий бромистый, кажущееся относительное молярное теплосодержание 501 Барий бромистый, коэффициент активности средний 397 530 Барий бромистый, относительное парциальное молярное теплосодержание 503 Барий гидрат окиси, константа диссоциации иона по данным электропроводности 149 Барий железистосинеродистый, электропроводность, влияние силы поля 209 Барий железосинеродистый, электропроводность, влияние силы поля 209 Барий йодистый, коэффициент активности средний 570 Барий хлористый, влияние на коэффициент • активности соляной кислоты 425—426 Барий хлористый, высаливание нейтральных молекул 376 377 Барий хлористый, кажущаяся молярная сжимаемость 264 Барий хлористый, кажущееся относительное молярное теплосодержание 501 Барий хлористый, кажущийся молярный объем 242 Барий хлористый, коэффициент активности средний 389 397 529—530 Барий хлористый, молярная электропроводность, таблица 157 Барий хлористый, относительная вязкость, предельный коэффициент наклона 170 Барий хлористый, относительное парциальное молярное теплосодержание 503 Барий хлористый, парциальная молярная теплоемкость 237\ Барий хлористый, эквивалентная электропроводность 498 Барий хлористый, эффективное давление 261 Барксдел 374 385 Барометрическая поправка водных растворов, таблица 290 Бартон 429 447 Батлер, Дж.А. 65 73 Батлер, Дж.П. 568 588 Батсон 214 Батчельдер 488 496 Баумштарк 410 416 Бахем 264 265 267 268 Бекман, Е. 283 Бекман, Ц. 243 266 Бекштрём 348 386 Бельчер 181 216 304 310 549 Бенедикт 380 385 Бензойная кислота, константа диссоциации, определение методом электропроводности 205 Бензойная кислота, константа кислотной диссоциации 579 Бензойная кислота, константа кислотной диссоциации максимальная 582 Бензойная кислота, коэффициенты высаливания 529 Бензол, коэффициент сжимаемости 259 Бенневитц 178/240 266 Бенсон 589 Бергман 267 Беркели 283 Бернал 261 267 383 385 493 496 574 588 Берри 362 385 Бехтольд 415 Бигельэйзен 589 Бикуорд 263 267 Бикфорд 178 181 549 589 Бильтц 385 551 Бингхэм 179 Бинс 450 495 Бирдж 96 116 118 137 315 337 554 588 589 Бирдсэлл 553 Бирон, Е. 417 Бирр 215 Битти 297 310 313 337 338 384 Биховский 226 265 Бланчерд 496 Блатц 576 589 Блэкман 283 Блюментрит 34 45 116 209 215 Боген 490—492 496 Боде 417 Боллингер, Г. 139 178 Боллингер, Д. 139 177 Бонино 222 265 Боннер 578 589 590 Борн 65 73 214 321 490 498 Борная кислота, pH 0,05н. раствора 306 Борная кислота, изменение термодинамических функций при диссоциации 476 Борная кислота, константа диссоциации 465 541 Борная кислота, константа диссоциации в растворах хлористого натрия 583 Борная кислота, константа диссоциации максимальная 546 Борная кислота, применение для определения стандартных потенциалов элементов 347 Боусфильд, Е. 385 Боусфильд, У. 267 353 385 Брайтон 450 495 Брамбог 447 Браун 181 310 340 341 367 382 384 385 549 567 589 Брекенридж 447 Брендель 245 Бренстед 32 177 300 310 365 369 385 413 414 417 418—420 432 435 441 447 Бресчиа 492 496 Бриджер 267 Бриджмэн 258 267 Бринкли, Р. 565 Бринкли, С. 266 268 307 310 463 495 496 555 557 563 585 588 Бринкман 589 Бриско 173 180 Бриттон 302 310 Брицке, Э.В. 226 Бродский, А.И. 4 23 50 61 167 267 412 416 444 Брокман 181 216 Бромистоводородная кислота, коэффициент активности, средний в растворах бромистых солей 537 Бромистоводородная кислота, коэффициент активности, средний в растворах галоидных солей щелочных металлов 424 Бромистоводородная кислота, коэффициент активности, средний в растворах солей 423—426 Бромистоводородная кислота, коэффициент активности, средний водных растворов, таблица 519 Бромистоводородная кислота, относительная парциальная молярная теплоемкость, таблицы 332 519 Бромистоводородная кислота, относительное парциальное молярное теплосодержание в растворах бромистых солей 426—427 Бромистоводородная кислота, относительное парциальное молярное теплосодержание, таблица 519 Бромистоводородная кислота, среднее расстояние сближения ионов 360 Бромистоводородная кислота, стандартный потенциал элемента, содержащего бромистоводородную кислоту 348 Бромистоводородная кислота, термодинамические свойства растворов 347—348 Бруинс 562 588 Брунауэр 576 588 Брэдшоу 140 141 152 160 169 178 179 180 558 589 Брэй, В. 146 156 178 180 185 214 418 447 Брэй, У. 398 399 400 416 Брюлль 181 Булок 178 Буферные растворы, значения рН, таблица 306 Буферные растворы, применение для определения констант диссоциации 463—469 Буферные растворы, применение при определении стандартных потенциалов 347 Буферные растворы, стандартные потенциалы, таблица 305 Буш 178 214 Бьен 197 214 215 Бьеррум 29 30 32 45 54 55 57—59 61 73 110 125 137 182 189 198 309 310 312 361 383 385 398 496 572 573 574 586 588 589 Бэдфорд 416 Бэйтс, Р. 392 393 396 397 416 495 551 552 586 589 590 Бэйтс, С. 429 447 Бэкер, Л. 183 214 Бэкер, О. 590 Бэлл 589 Бэнкс 178 Бэр 468 Бэртон, Дж. 552 Бэртон, Ц. 283 Ваглио 222 265 Вагнер, К. 139 177 Вагнер, Ц. 70 73 178 380 382 Вазастьерна 137 Ваймен 119 137 228 229 265 368 385 496 Вайнел 413 414 417 Валентность, фактор, значение для коэффициентов активности 121—123 Валентность, фактор, значение для электропроводности 131 Валледдер 229 266 Вальде 479 496 Вальден 142 155 178 184 189 192 194 214 Ван-Лаар 33 45 271 283 Ван-Риссельберге 176 180 360 370 371 385 573 Ванзелов 283 322 338 Вернон 116 171 179 Вероятность нахождения иона в поле другого иона см. «Теория образования ионных пар» Веселовский, Б. 226 Виземан 385 Вильсон, Дж. 417 Вильсон, Р. 267 Вильсон, У. 34 45 101 105 116 135 Вильямс 179 Вин 116 205 206 208 210 215 Вин-Джонс 177 475 476 479 491 494 496 Винджи 214 283 Виноград 177 180 Винцент 266 Вирт 241 266 268 Вода, активность в водных растворах серной кислоты, определение 408—410 Вода, активность в водных растворах серной кислоты, определение по данным измерений электродвижущих сил и упругости пара 409 Вода, активность в растворах серной кислоты, таблица 409 Вода, диссоциация в растворах солей 454—457
Реклама
 |
|
О проекте
|
|
О проекте



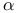 -Динитрофенол, константа диссоциации, определение
-Динитрофенол, константа диссоциации, определение