Авторизация
Поиск по указателям
Арбузов Ю.Н. (ред.) — Органические реакции (т. 8)
Обсудите книгу на научном форуме Нашли опечатку?
Название: Органические реакции (т. 8)Автор: Арбузов Ю.Н. (ред.) Аннотация: Первая статья сборника посвящена каталитической гидрогенизации сложных эфиров в соответствующие спирты при помощи медно-хромового катализатора Адкинса и никелевого катализатора Ренея. Этот метод каталитической гидрогенизации имеет ряд существенных преимуществ перед старым методом Буво и Блана и в настоящее время находит широкое применение в лабораториях. Важному методу синтеза кетонов из галоидангидридов кислот и металлоорганических соединений магния, цинка и кадмия посвящена вторая статья.
Язык: Рубрика: Химия /Статус предметного указателя: Готов указатель с номерами страниц ed2k: ed2k stats Год издания: 1956Количество страниц: 580Добавлена в каталог: 18.09.2006Операции: Положить на полку |
Скопировать ссылку для форума | Скопировать ID
Предметный указатель
Перегруппировка 1-ацетокси-2-ацетилнафталина 120 Перегруппировка 2-ацилокси- и 2-ароилоксикетонов, таблица 218—225 Перегруппировка 2-пальмитоилокси-1-ацетилнафталина 120 Перегруппировка бензилметилового эфира в литиевый алкоголят фенилметилкарбинола 352 Перегруппировка дибензилового эфира в алкоголят фенилбензилкарбинола 352 Перегруппировка сложных эфиров 9-флуорениловых эфиров 352 Перегруппировка сложных эфиров o-оксиацетофенонов 118—120 123 Перегруппировка сложных эфиров метил-o-оксиарилкетонов 119 Перфтормасляной кислоты альдегид, восстановление по методу Розенмунда 328 Пиридин-3-альдегид, получение 277 Пиролины 486 487 488 Пиролины пиролиз 487 Превращение галоидометильной группы в альдегидную по реакции Крёнке 268 Превращение галоидометильной группы в альдегидную при взаимодействии замещенных галоидных бензилов с натриевой солью 2-нитропропана 268 Превращение сложных эфиров в спирты в результате гидрогенизации 7 Превращение сложных эфиров в спирты в результате гидрогенолиза 7 Пропилидендиацетат 134 Пропионилацетон 101 Пропионилацетон синтез 141 Пропионилпировиноградной кислоты этиловый эфир, получение 147 148 Пропионовая кислота, самоконденсация 130 Пропиофенон, синтез 52 Реагенты, применяемые для разложения нитрозосоединения 495 Реакции диазометана и его производных, аппаратура 500 501 Реакции диазометана и его производных, влияние катализатора 497 Реакции диазометана и его производных, влияние концентрации реагентов 498 Реакции диазометана и его производных, влияние растворителей 496 497 Реакции диазометана и его производных, влияние температуры 498 Реакции кетона с хинонами 406 Реакции кетона с хинонами в присутствии катализатора, таблица 435 Рейссерта соединения, гидролиз 291 Рейссерта соединения, получение 291 Рейссерта соединения, схема разложения 289 Ртути (II) соли, металлирующин агент 357 Синтез из 397 Синтез из 397 Синтез из 397 Синтез из 395 Синтез из дифенилкетена хинодиметана 399 Синтез методом восстановительного обессеривания эфиров тиоловых кислот 300 302 Синтез методом восстановительного обессеривания эфиров тиоловых кислот 300 Синтез методом восстановительного обессеривания эфиров тиоловых кислот бензальдегида 299 Синтез методом восстановительного обессеривания эфиров тиоловых кислот тетрацетата аль-дегидо-D-рибозы 299 Синтез методом Грундмана 10-гендеценаля 296 297 298 Синтез методом Грундмана 3-бензилокси-4-метоксифенилацетальдегида 295 296 Синтез методом Зонна и Мюллера 1,2,3,4-тетрагидро-9-фенантральдегида 312 Синтез методом Зонна и Мюллера 1-, 2-, 3- и 9-фенантральдегидов 311 Синтез методом Зонна и Мюллера 3,4,5-триметоксибензальдегида 311 Синтез методом Зонна и Мюллера 3,5-диметоксибензальдегида 311 Синтез методом Зонна и Мюллера 3-фенантрен-3-альдегида 316 Синтез методом Зонна и Мюллера n-хлорбензальдегида 312 Синтез методом Зонна и Мюллера o-толуилового альдегида 311 Синтез методом Зонна и Мюллера бензальдегида 312 Синтез методом Зонна и Мюллера коричного альдегида 311 313 Синтез методом Зонна и Мюллера фенантренальдегида 316 Синтез методом Мак-Фадиена и Стивенса 1,3,5-тринитробензола 303 Синтез методом Мак-Фадиена и Стивенса 4-амино-2-метилпиримидин-5-альдегида 305 310 Синтез методом Мак-Фадиена и Стивенса 6- и 4-метилциклогептатриенонов 303 Синтез методом Мак-Фадиена и Стивенса n-(n'-метоксифенокси)бензальдегида 305 Синтез методом Мак-Фадиена и Стивенса бензальдегида 304 305 Синтез методом регулируемого восстановления 324 Синтез методом регулируемого восстановления 324 Синтез методом регулируемого восстановления 325 Синтез методом регулируемого восстановления 324 Синтез методом регулируемого восстановления 9-фенилнонатетраеналя 325 Синтез методом регулируемого восстановления циннамилиденацетальдегида 324 Синтез методом Стефена 319 323 Синтез методом Стефена 3,5-дииод-4-(4'-метоксифенокси)бензальдегида 323 Синтез методом Стефена 4-метилтиазол-5-альдегида 323 Синтез по реакции Соммле 1-нафтальдегида 276 Синтез по реакции Соммле 2-толуилового альдегида 275 Синтез по реакции Соммле 2-фенилтиазол-4-альдегида 267 Синтез по реакции Соммле 3,5-дихлор-2-оксибензальдегида 266 Синтез по реакции Соммле 3-хлор-4-оксибензальдегида 266 Синтез по реакции Соммле 4-метоксиизофталевого альдегида 278 Синтез по реакции Соммле n-нитробензальдегида 276 Синтез по реакции Соммле o-иодбензальдегида 276 277 Синтез по реакции Соммле алифатических альдегидов 267 Синтез по реакции Соммле алифатических и арилалифатических альдегидов, таблица 279 Синтез по реакции Соммле ацетофенона 268 Синтез по реакции Соммле бензофенона 268 Синтез по реакции Соммле гетероциклических альдегидов 267 Синтез по реакции Соммле гетероциклических альдегидов, таблица 283 Синтез по реакции Соммле диальдегидов 267 Синтез по реакции Соммле диальдегидов, таблица 284 Синтез по реакции Соммле замещенных бензальдегидов, таблица 280—281 Синтез по реакции Соммле изовалерианового альдегида 267 Синтез по реакции Соммле кетонов 268 Синтез по реакции Соммле н-гексилового альдегида 267 Синтез по реакции Соммле н-гептилового альдегида 267 277 278 Синтез по реакции Соммле н-масляного альдегида 267 Синтез по реакции Соммле нитрооксибензальдегидов 266 Синтез по реакции Соммле пиридин-3-альдегида 267 277 Синтез по реакции Соммле полициклических альдегидов, таблица 282 Синтез по реакции Соммле тиофен-2-альдегида 267 Синтез по реакции Соммле триметилацетальдегида 267 Синтез по реакции Соммле фенилацетальдегида 267 Синтез по реакции Соммле флуоренона 268 Синтез через стадию образования соединения Рейссерта 1-скатилизохинолина 290 Синтез через стадию образования соединения Рейссерта 5-фенилпентадиеналя 290 Синтез через стадию образования соединения Рейссерта 6-метоксихинолин-2-карбоновой кислоты 290 Синтез через стадию образования соединения Рейссерта o-нитробензальдегида 292 Синтез через стадию образования соединения Рейссерта изохинолин-1-карбоновой кислоты 290 Синтез через стадию образования соединения Рейссерта изохинолинов 291 Синтез через стадию образования соединения Рейссерта коричного альдегида 290 Синтез через стадию образования соединения Рейссерта лепидина 291 Синтез через стадию образования соединения Рейссерта тетрагидроизохинолина 290 Синтез через стадию образования соединения Рейссерта фенантридин-6-карбоновой кислоты 290 Синтез через стадию образования соединения Рейссерта хинолин-2-карбоновой кислоты 290 Соммле реакция 263—287 Соммле реакция, влияние кислотности раствора 273 274 Соммле реакция, выбор растворителя 271—273 Соммле реакция, механизм 264—265 Соммле реакция, область применения 266—=268 Соммле реакция, побочные реакции 274 Соммле реакция, препаративные синтезы 275— 278 Соммле реакция, рекомендуемая методика 274 Соммле реакция, родственные реакции 268-269 Соммле реакция, таблицы 279—285 Сорбиновой кислоты этиловый эфир получение через 408 Стефана метод 316—324 Таллия хлорид, металлирующий агент 357 Теллура хлорид, металлирующий агент 357 Тетра(и пента)металлирование толуола 340 Тетраметаллирование дифенилметана 340 Тетрацетаты D- и L-1-дезоксифруктоза 475 Тиоловых кислот сложные эфиры, получение 299 300 Тиофен-2-альдегид 267 273 Тиофенол 348 трет-Бутилат калия, конденсирующий агент при ацилировании 117 Три-o-фенилен 342 Тридеканол 315 Триметил( 344 Триметилбетаин 418 419 Трифенилметилкалий, конденсирующий агент при ацилировании 140 Трифенилметиллитий 339 Трифенилметилнатрий, конденсирующий агент при ацилировании 92 94 96 109 140 Трифторметилдиазометан, получение 492 Триэтиламин, конденсирующий агент при ацилировании 122 Триэтиламин, применение при гидрогенизации 36 Уксусная кислота, растворитель при проведении реакции Соммле 272 Уксусный ангидрид, самоконденсация 129 130 Уротропин 263 272 273 274 275 276 277; Уротропиновые соли 263 264 269 270 273 274 275 276 277 278 Уротропиновые соли, выделение 270 Уротропиновые соли, получение 270 271 Фенантрен-2-альдегид, получение 316 Фенантрен-3-альдегид, получение 316 Фенантридин 290 Фенилацетилен 342 Фенилдиазометан, взаимодействие с циклогексаноном ex situ в присутствии катализатора 503 504 Фенилдиазометан, взаимодействие с циклопентаноном 484 Фенилдиэтиламин 342 Фенилкальций иодистый, металлирующий агент 357 Фениллитий, металлирующий агенг 338 340 341 342 343 345 352 354 355 358 361 362 Фениллитий, получение 360 Феноксидибензоилметан 107 Флавоны 119 120 121 123 269 Флавоны, синтез по реакции Дуффа 269 Флуорен 338 339 Флуорен-9-карбоновая кислота 338 Формилирование в присутствии щелочных агентов 2-оксифенилбензилкетона 117 Формилирование в присутствии щелочных агентов ацетона 116 Формилирование в присутствии щелочных агентов гидриндона-1 117 Формилирование в присутствии щелочных агентов диэтилкетона 117 Формилирование в присутствии щелочных агентов камфоры 117 Формилирование в присутствии щелочных агентов кетонов стероидного типа 117 Формилирование в присутствии щелочных агентов метил-н-пропилкетона 116 Формилирование в присутствии щелочных агентов метилизобутилкетона 116 Формилирование в присутствии щелочных агентов метилэтилкетона 116 Формилирование в присутствии щелочных агентов полигидрофенантренов 117 Формилирование в присутствии щелочных агентов циклопентанона 117 Фриса реакция 134 Хинолин-2-карбоновая кислота 289 Хлор-3,5-диметоксибензальдегид 315 Хлорбензальдегид, образование через соединение Рейссерта 289 Хромоны 118 120 121 122 123 Циклизация 123 124 Циклизация Дикмана 105 Циклогексанон, самокондеисация 95 Циклогептанон, получение методом in situ 504 Цинк хлористый, применение для приготовления цинкорганических соединений 46 47 Цинк-хромовый катализатор гидрогенизации 36 Цинкорганические соединения, получение 46 Цинкорганические соединения, реакция с галоидангидридами кислот 49 50 Штоббе реакция 96 Эквиленин 115 149 Этандиол-1 211 Этил-2-фурилкетон, получение 501 Этиламид никотиновой кислоты 312 Этилат натрия, конденсирующий агент при ацилировании 90 91 93 94 96 98 99 103 104 105 106 107 108 109 111 112 116 117 118 120 123 139 140 144 145 146 Этилацетат, самокоиденсация 96 Этилиатрий, металлирующий агент 356 Этилкалий, металлирующий агент 356 Этиллитий, металлирующий агент 333 339 340 356 358 Этилмагний бромистый, конденсирующий агент при ацилировании 140 Этиловый спирт, растворитель при проведении реакции Соммле 271 272
Реклама
 |
|
О проекте
|
|
О проекте



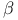 -галоидодамещенных кислот
-галоидодамещенных кислот 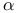 -метил-
-метил-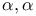 -дифенил-
-дифенил-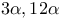 -диацетоксинорхоланаля-23
-диацетоксинорхоланаля-23 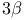 -ацетоксихолен-5-аля-24
-ацетоксихолен-5-аля-24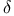 -метиламиновалерианового альдегида
-метиламиновалерианового альдегида 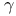 -диметиламино-
-диметиламино-